红细胞系统疾病
一、贫血总论
贫血的定义(掌握)
贫血的分类(掌握)
贫血的病因(掌握)
贫血的表现(熟悉)
贫血的诊断(熟悉)
贫血的治疗原则(了解)
一、贫血(anemia)定义
➢ 由各种原因引起的外周血中血红蛋白量(HB),红细胞计数(RBC)及红细胞容量(HCT)减少,低于相同年龄,性别及地区的正常下限,不能运输足够的氧至组织而产生的综合征。
➢ 由于红细胞容量测定复杂,临床上以血红蛋白量的减少作为贫血最为重要的标准
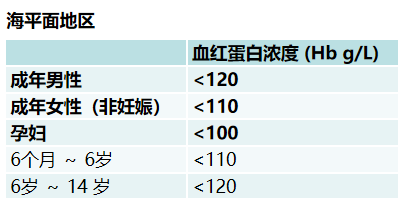
(海拔增高,需要氧气浓度更高,浓度增高)
(小孩刚出生时,氧含量增加,红细胞生成下降)
贫血的影响因素
➢ 居住地海拔:
➢ 性别:
➢ 年龄:
➢ 血容量的改变:
贫血分类
1) 贫血的进展速度:

2) 贫血严重程度:
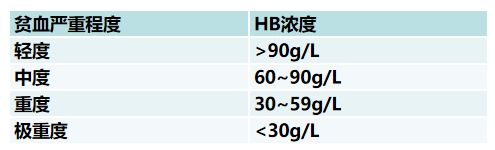
3) 细胞形态学:
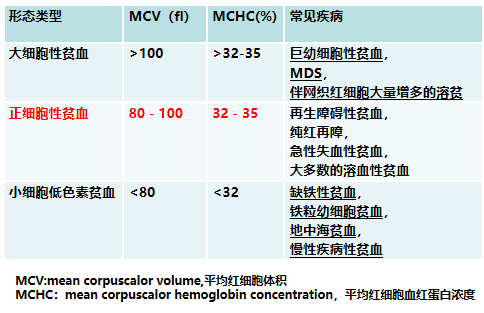
4) 骨髓增生情况:

5) 贫血病因:
一、红细胞生成减少
(1)造血细胞的增生和分化异常:再障,白血病,骨髓瘤,MDS
(2)造血微环境异常:转移癌,骨髓纤维化
(3)造血调节异常:再障,肾性贫血,肿瘤
(4)造血物质缺乏或利用障碍:缺铁性贫血,巨幼贫,铁利用障碍
二、红细胞破坏过多——溶血性贫血
(一)红细胞内源性异常
(1)红细胞膜缺陷:遗传性球形/椭圆形红细胞增多症
(2)酶缺陷:G-6-PD缺乏,丙酮酸激酶缺乏
(3)珠蛋白异常:地中海贫血,镰状细胞贫血
(4)血红素异常:铅中毒、卟啉病
(二)红细胞外源性异常
1、免疫性因素
• 自身免疫性溶血性贫血 AIHA
• 新生儿溶血症(Rh,ABO)
• 血型不符的输血反应
2、血管性因素:
①微血管病性HA:血栓性血小板减少性紫癜TTP(不常见)
②瓣膜病:主动脉狭窄、心脏瓣膜置换术后
③血管壁受反复挤压:行军性血红蛋白尿
3、生物因素:疟疾
4、理化因素:大面积烧伤、亚硝酸盐中毒
三、失血性贫血
➢ 出凝血疾病:
• 与血小板减少有关: 免疫性血小板减少性紫癜
• 与凝血因子缺乏有关:血友病,严重肝病
➢ 非出凝血疾病:
• 良性:消化道溃疡,子宫肌瘤,宫外孕破裂,痔疮,结核
• 恶性:消化道肿瘤,肺癌,泌尿道肿瘤
贫血的临床表现
➢ 各系统缺氧表现
• 肌肉:疲乏无力,最常见,最早出现的症状。
• 皮肤黏膜:苍白、黄疸。
• 循环系统:活动后心悸,是循环系统最突出的症状。心动过速,心尖区可及收缩期杂音,即贫血性杂音。严重贫血可导致心绞痛,心衰,体位性低血压。
• 呼吸系统:活动后气促。
• 神经系统:头晕,耳鸣,嗜睡,注意力及记忆力下降。异食癖。严重贫血或急骤发生的贫血,可导致晕厥。
• 消化系统:食欲减退,镜面舌(舌乳头萎缩),plummer-vinson综合征(缺铁性吞咽困难)。
• 泌尿系统:蛋白尿,少尿,酱油色尿,铁锈色尿,鲜血尿(泌尿道结石、肿瘤)。
• 生殖系统:月经失调
➢ 原发病的表现:
消化道溃疡:球溃可有空腹时腹痛,进餐后缓解
子宫肌瘤:月经量增多
急性白血病:伴随发热,出血,浸润症状
多发性骨髓瘤:骨痛,病理性骨折
贫血症状的影响因素
1贫血的严重程度:
2贫血发生的速度:
3体力活动:活动后缺氧更重
4机体对贫血的代偿能力: 代偿能力差导致缺氧加重
Q:为何慢性贫血症状轻?
A: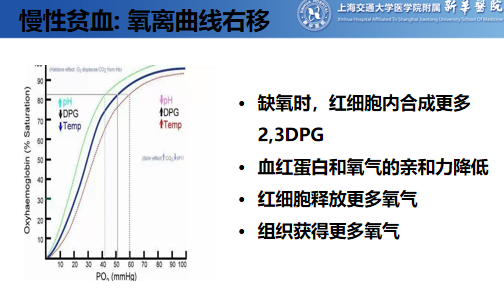
(DPG——二磷酸甘油酸)
贫血的诊断
(一)详细询问病史
• 贫血的症状:头晕乏力,活动后心悸气促
• 贫血发生的时间,病程,速度,程度,诱因
• 出血史/饮食史/既往史/手术史(尤其消化道)/理化接触史(放射性、化疗药物)/家族史/月经史/孕产史
• 地域分布:
• 检查+治疗+疗效:
(二)体格检查
• 皮肤苍白,黄染,瘀斑瘀点
• 反甲(严重缺铁性)
• 舌乳头萎缩(B12缺乏)
• 胸骨压痛(白血病)
• 心率、心脏杂音
• 肝脾,淋巴结肿大,肿块
• 肛门指检
• 妇科检查
(三)实验室检查
➢ 血常规检查:
RBC计数,HB,MCV,网织红细胞,WBC计数,血小板计数,异常细胞形态
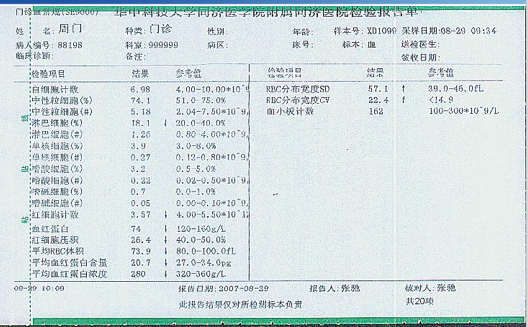
➢ 血涂片
• 外周血涂片:观察红细胞形态有无异常
• 正常红细胞形态:双凹圆盘状,这样的红细胞表面积较大,变形能力强,容易穿越脾脏微循环。
• 异常红细胞:球型,椭圆型,口型,破碎,镰状(不容易被破坏)
• 红细胞缗钱状排列:MM(原发性骨髓瘤)
• 中心淡染区扩大:IDA
常细胞形态
➢ 骨髓检查:
骨髓涂片
• 增生度,细胞分类,细胞形态
• 铁染色
• 细胞化学染色
流式(白血病/骨髓瘤免疫分型)
细胞遗传学/分子生物学
骨髓病理活检
• 骨髓增生度
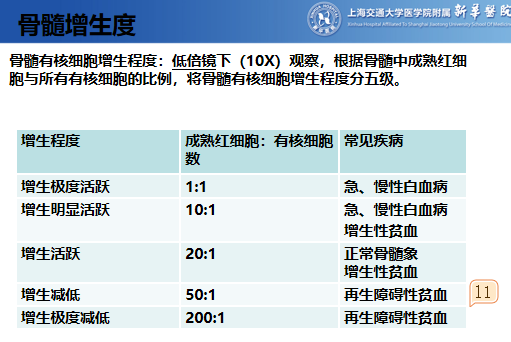
• 造血组织分布和面积
• 骨髓纤维化
• 肿瘤转移
➢ 尿常规,粪常规+隐血
➢ 生化检查:肝肾功能;甲状腺功能;血清铁,总铁结合率,铁蛋白;血清叶酸,维生素B12浓度;
➢ 溶血相关检查:红细胞渗透脆性试验,PNH筛查,G-6-PD酶活性测定,血红蛋白电泳,coomb’s test
➢ 免疫学检查:ANA系列
➢ 影像学检查:B超,CT/MRI,PET-CT
➢ 病理活检检查:
胃肠镜/支气管镜/鼻咽镜/腹腔镜
淋巴结活检
治疗(不重要的)
一、病因治疗
去除病因是治疗贫血的关键。
贫血病因未明确前,不要随意用药。
➢ 补充造血原料:
缺铁贫:铁剂 ;
巨幼贫:叶酸,维生素12
➢ 刺激造血的生长因子和药物:
再障:雄激素;
肾病:红细胞生成素
➢ 免疫抑制剂:
再障、溶血等:糖皮质激素, 环孢素,ATG
化疗、放疗:肿瘤性疾病
➢ 造血干细胞移植:
骨髓瘤,淋巴瘤,急性白血病,MDS
再障,地中海贫血
➢ 手术:
切脾:遗传性球形红细胞增多症;AIHA;ITP
切除胸腺瘤:胸腺瘤导致的纯红再障:
二、对症治疗
➢ 输血:
• 慢性贫血HB<60 g/L是输血指征。
• 急性大量失血者,及时输血,恢复血容量。
• 重度贫血、合并心肺功能不全的贫血患者,输红细胞,可改善体内缺氧状态;
• 长期大量输血导致铁过载,予以祛铁治疗。
➢ 止血:
• 根据出血机制的不同予以相应的止血治疗
• 消化道溃疡予以制酸剂
• 血小板减少应输血小板;
• 凝血因子缺乏应补充凝血因子
➢ 避免接触溶血诱发因素:
• 药物引发溶血,立即停药,避免再次用药;
• G6PD酶缺乏,避免食用蚕豆及氧化剂
• 冷抗体型AIHA,注意保暖
• 溶血性贫血,不宜输普通红细胞
思考题
贫血的病因?
如何诊断贫血?
贫血的治疗?
二、缺铁性贫血(IDA)
1.掌握缺铁性贫血的病因、临床表现和实验室检查特点。
2.掌握缺铁性贫血的防治原则。
概述
• 缺铁性贫血是因机体对铁的供需失衡,贮存铁耗尽,血红蛋白合成减少,而引起小细胞低色素性贫血。
• IDA是最常见的贫血。尤其是欠发达地区。
• 女性多于男性。好发于婴幼儿,育龄妇女。
铁的代谢
铁的来源
• 外源性途径供铁:膳食,药物
• 内源性途径供铁:主要来自于衰老和破坏的红细胞释放的铁。是外源性途径的15-20倍。
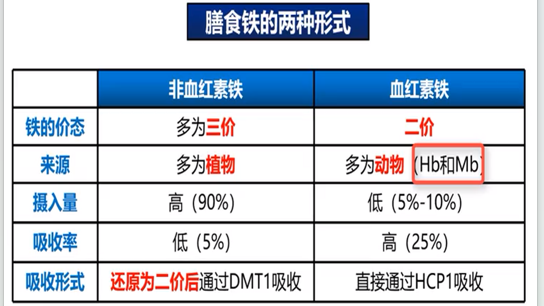
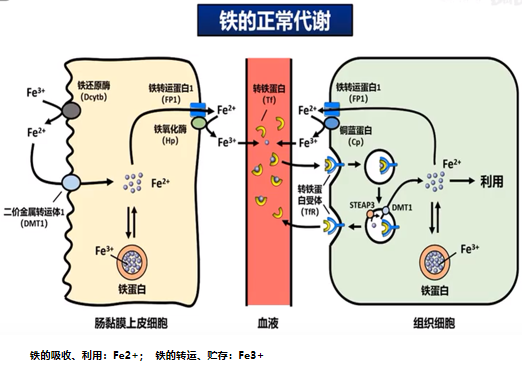
铁的代谢
铁的吸收:
• Fe2+
• 十二指肠及空肠上段
• 干扰因素:浓茶,钙,氧化剂
• 铁的口服吸收量与贮存量呈负相关。
铁在血液中的转运:
• Fe3+
• 转铁蛋白
铁的利用:
• Fe2+。
• 肠外组织摄铁形式:经转铁蛋白受体入胞。
• 摄铁的主要细胞:骨髓红系细胞,用于合成血红蛋白。此外,铁还参与合成含铁酶,铁依赖酶。
铁的贮存:
• 铁蛋白Fe3+ (水溶性),含铁血黄素(非水溶性),
• 主要储存在单核巨噬细胞、肝细胞。
铁的分布:
功能铁 :80%
血红蛋白 70%(主要在骨髓的幼红细胞内合成)
肌红蛋白 10%
铁依赖酶
转铁蛋白
贮存铁 :20%
贮存部位:肝、脾、骨髓。正常人血清中含量很少。
贮存形式:血清铁蛋白: Fe3+,溶于水,易再利用。
含铁血黄素:难溶于水,难再利用。
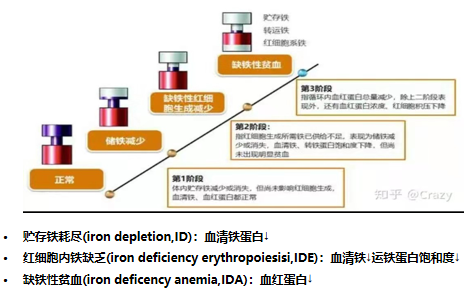
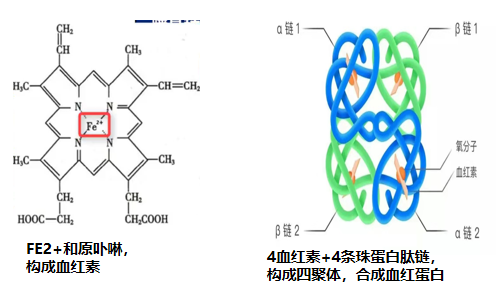
血红蛋白的结构
IDA病因
➢ 需求增加、摄入不足:儿童、孕产妇
➢ 吸收障碍:如胃大部切除术后
➢ 丢失过多:如慢性胃肠道失血(钩虫病、痔疮、消化性溃疡、肿瘤等),月经过多。慢性失血是IDA最常见的病因。

➢ IDA高发地区:
经济欠发达地区
钩虫病流行地区
➢ IDA高发人群:
婴幼儿
育龄妇女
临床表现
1、贫血一般表现:
头晕,乏力,苍白
2、缺铁原发病表现:
子宫肌瘤(月经量增多);
消化道溃疡(腹痛,黑便);
肿瘤(消瘦、大便性状改变)
3、组织缺铁表现:
①生长发育迟缓:核苷酸还原酶活力降低,导致细胞增殖迟缓,生长速度减慢;
②神经、精神系统异常:注意力涣散,记忆力减退,理解力降低,激惹,攻击性行为,智商下降,异食癖;
③肌肉系统:肌力下降;
④消化系统:舌炎、嘴角炎;plummer-vinson综合征(缺铁性吞咽困难);
⑤内分泌系统:T4 、T3 障碍;
⑥免疫系统:细胞免疫能力下降;
⑦ 指甲:易脆,反甲。
实验室检查
1、血象
红细胞数量减少;
红细胞体积小或大小不一;
着色浅,中心淡染区扩大(血红蛋白减少),严重者呈环形;
钩虫病引起的IDA,嗜酸性粒细胞增高。
2、骨髓象:IDA“老核幼浆”现象
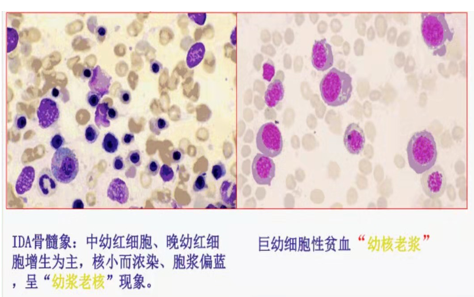

3、骨髓铁染色:细胞外铁阴性
1.血清铁蛋白(SF)↓(贮存铁↓)<15ug/L
2.血清铁(SI)(转铁蛋白结合铁)↓<10.7umol/L
转铁蛋白饱和度(TS)↓<15%
总铁结合力(TIBC)↑ >64umol/L
总铁结合力(TIBC)=血清铁(SI)÷转铁蛋白饱和度(TS)
3.原卟啉FEP↑
4、铁代谢
1.血清铁蛋白(SF)↓(贮存铁↓)<15ug/L
2.血清铁(SI)(转铁蛋白结合铁)↓<10.7umol/L
转铁蛋白饱和度(TS)↓<15%
总铁结合力(TIBC)↑ >64umol/L
总铁结合力(TIBC)=血清铁(SI)÷转铁蛋白饱和度(TS)
3.原卟啉FEP↑
诊断及鉴别诊断
IDA诊断标准
• 具有明确的缺铁原因
• 临床表现(贫血、原发病、组织缺铁的表现)
• 外周血:红细胞呈小细胞低色素性,MCV<80fl MCHC<31%
• 骨髓涂片:老核幼浆,胞浆蓝染
• 铁染色:骨髓细胞外铁明显减少
• 铁代谢指标:血清铁蛋白(SF)↓,血清铁(SI)↓转铁蛋白饱和度(TS)↓,总铁结合力(TIBC)↑
• 铁剂治疗有效:治疗4周后Hb应上升20g/L以上
• 排除:其他小细胞低色素性贫血
IDA诊断步骤
1是否有贫血?
2贫血程度?
3是否是IDA?
4缺铁的病因?
鉴别诊断
1.铁粒幼细胞性贫血
• 小细胞性贫血
• 遗传或不明原因导致的获得性的红细胞铁利用障碍性贫血。染色体核型异常。
• 出现环形铁粒幼细胞。
• 血清铁蛋白↑、血清铁↑ 、骨髓外铁及内铁↑ 、铁饱和度↑总铁结合力↓
2.海洋性贫血
• 有溶血表现,肝脾肿大,黄疸
• 有家族史
• 血片:多量靶形红细胞
• 珠蛋白肽链合成数量异常:
血红蛋白电泳异常 HbF↑、HbA2↑
• 血清铁蛋白↑ 、骨髓可染铁↑ 、血清铁↑ 、
• 铁饱和度↑总铁结合力↓
3.慢性病性贫血
• 慢性感染,恶性肿瘤,风湿病,肝病,肾病,内分泌疾病等伴发的贫血。
• 铁累积于单核-巨噬系统内,造成可循环利用的铁量减少。
• 血清铁↓(必备条件)总铁结合率↓ 铁饱和度↓
• 血清铁蛋白↑骨髓细胞外铁↑
• 可溶性运铁蛋白受体不升高
IDA的防治
预防
• 缺铁高危人群:孕妇、哺乳期妇女、早产儿、低出生体重儿,可通过药物铁、铁强化食物或增加营养摄取足够铁元素以预防缺铁性贫血。
• 哺乳期妇女提倡母乳喂养。
• 婴幼儿及时添加含铁丰富且铁吸收率高的辅食。
• 饮食中有足够的动物性蛋白和豆类食物,不仅可提供优质蛋白质,其铁含量较高,吸收率也较高。鸡鸭血、猪血也是铁的良好来源。豆浆较牛奶供铁量更高。每天需摄入足够量的新鲜水果或蔬菜,以供给维生素C而促进铁的吸收。
• 积极治疗可能引起缺铁性贫血的各种原发病(慢性出血性疾病、肿瘤等)。
• 缺铁高危人群定期筛查。
治疗
根除病因,补足贮铁
病因治疗
(1)婴幼儿,妊娠妇女:调整饮食
(2)寄生虫:驱虫
(3)恶性肿瘤:手术,化疗
(4)消化道溃疡:制酸
补铁治疗
①首选口服铁剂:
➢ 常用口服铁剂:
无机铁:硫酸亚铁
有机铁:右旋糖酐铁,多糖铁复合物等
➢ 注意事项:
胃肠道反应:饭后服用,减少胃肠道刺激。
牛奶、茶、咖啡及抗酸药等与铁剂同服均可影响铁的吸收。不和茶,咖啡,牛奶同服。
同时服用维生素C,可增加铁的吸收。
胃大部切除者,不适用口服补铁。
②注射铁剂
➢ 适应证:
口服铁剂不耐受:严重消化道反应,无法耐受;胃大部切除者,消化道吸收障碍。
妊娠晚期,铁需求量增加。
➢ 常用注射铁剂:右旋糖酐铁 肌注;蔗糖铁(临床上多用) 静滴
➢ 注射用铁的剂量应准确计算,公式为:
所需补充铁的量(mg) = ( 150-患者Hb) X体重(kg)XO. 33
➢ 注意事项:
注意过敏反应:如皮肤潮红,荨麻疹,发热,关节痛
③铁剂治疗反应:
网织红细胞 3-4天上升,5-10天达高峰;
HB 2周后上升;2月完全恢复正常
④疗程:Hb正常后还要补足贮存铁,继续口服3~6月
补铁治疗后,HB不升的原因
剂量不足
吸收不良
损失大于补充
药物含铁不足
诊断错误
思考题
- IDA 的病因?
- IDA如何诊断?(临床表现,实验室检查)
- IDA的治疗原则?
三、再生障碍性贫血(AA)
再障的定义
再障的病因及发病机制
再障的分型
再障的临床表现,实验室检查
再障的诊断标准,鉴别诊断
再障的治疗
(一)定义
再生障碍性贫血,简称再障(Aplastic anemia,AA),是一种由不同病因和机制引起的骨髓造血功能衰竭。主要表现为 全血细胞减少, 贫血、出血和感染。免疫抑制治疗有效。
(主要病因:免疫功能亢进)
全血细胞减少的原因
• 骨髓造血功能衰竭(HSC的质、量缺陷)
• 骨髓占位(白血病、骨髓瘤、淋巴瘤、骨髓转移性肿瘤等异常细胞浸润或骨髓纤维化,占据正常造血细胞的空间)
• 骨髓受抑(化疗、辐射、感染等)
• 原料缺乏(巨幼贫)
• 破坏过多(脾亢,SLE)
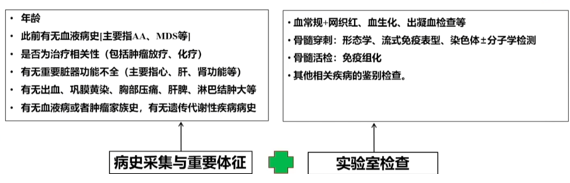
(全血细胞减少的诊疗流程)
流行病学
发病率:
欧美 0.47/10万人口
我国 0.74/10万人口
日本1.47 /10万人口
年龄:
亚洲地区中青年居多,欧美以老年人居多。
(二)分型
1、按遗传分:
后天获得性
先天性(占80%-88%,病因不明)
2、按病因分:
原发性:无明确病因
继发性:有明确病因,如药物、射线、感染
3、按病情分:
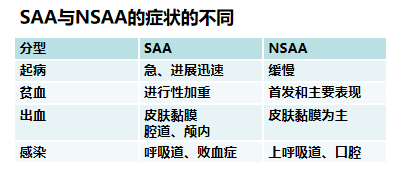
重型再障(SAA)
极重型再障(VSAA)
非重型再障(NSAA)
4、按病程分:
AAA(SAA-Ⅰ)
CAA(NSAA)
(三)病因
1病毒感染:特别是肝炎病毒,微小病毒B19等。
2化学因素:氯霉素,苯,磺胺药,抗肿瘤药,染发剂等。
3物理因素:放射性核素、X射线。
4妊娠:欧美国家多见

(免疫是主要机制)
(四)临床表现
➢ 贫血:与出血不一致
➢ 出血:
• 皮肤黏膜出血
• 腔道出血(呼吸道,消化道,泌尿道,生殖道等)
• 颅内出血
➢ 感染:
• 呼吸道感染最常见
• 败血症
(五)实验室检查
1、血象
1全血细胞减少:正细胞正色素性贫血
2淋巴细胞比例:明显增高
3网织红细胞:↓ 百分数多在0.5%以下,绝对值<15X10^9/L
4血小板计数:↓ <20X10^9/L
5细胞形态:白细胞、红细胞形态无明显异常,无异常、幼稚细胞
2、骨髓涂片及活检
• 骨髓增生减低,有核细胞显著减少。
• 粒系、红系减少、巨核系减少
• 非造血细胞比例增加:淋巴细胞,浆细胞,网状细胞,脂肪细胞,组织嗜碱细胞增多。
• 骨髓小粒空虚。
• 骨髓活检:骨髓脂肪变,呈空网状
骨髓小粒
正常小粒:
由基质细胞、网状纤维构成的造血支架,支架内散在生长着造血细胞。
小粒空虚:
仅见非造血细胞和网状纤维构成的空支架,而造血细胞少见
(六)诊断及分型
AA的诊断标准

AA的分型标准

(七)鉴别诊断
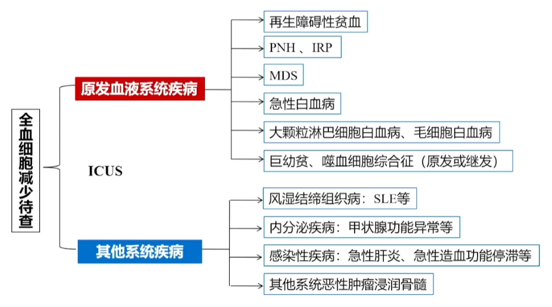
(会导致全血细胞减少的原因)
1、范科尼贫血(FA)
又称先天性AA,是常染色体或X连锁隐性遗传病。
表现为先天性畸形(骨骼畸形、器官发育不全等),骨髓衰竭,肿瘤易感。
造血干细胞移植可根治。
2、阵发性睡眠性血红蛋白尿(PNH)
获得性克隆性红细胞膜的缺陷
慢性血管内溶血性疾病,与再障可相互转变
临床表现:睡眠相关的血红蛋白尿,血栓,骨髓衰竭
补体调节蛋白异常表达:CD55↓CD59↓
FLAER试验:GPI阴性(书上没有,应该没那么重要?)
酸溶血试验(Ham Test):阳性

3、骨髓增生异常综合症MDS
造血干细胞克隆性疾病,向AML转化风险。
多数骨髓增生活跃,骨髓细胞分化障碍,细胞分化停滞在较早阶段,可见一系或多系病态造血。原始细胞比例增多。
MDS中的难治性贫血,可有全血细胞减少,网织红细胞降低,骨髓低增生。
大细胞性贫血。
4、低增生白血病
除了有贫血,出血,感染,还有浸润症状及体征。
骨穿:某系原始+幼稚细胞>20%
5、大颗粒淋巴细胞白血病

6、噬血细胞综合征

7、自身抗体介导的全血细胞减少症
包括Evans综合征和免疫相关性全血细胞减少。
机制:B淋巴细胞功能亢进,产生针对骨髓或外周血细胞的抗体,进而抑制或破坏造血,导致全血细胞减少。
网织红细胞不低或增高。
对糖皮质激素、CSA、大剂量丙球、CD20单抗或CTX治疗反应较好。
8、急性造血停滞
获得性:多种感染(以微小病毒B19多见)或药物可诱发急性造血停滞,以微小病毒B19多见。
骨髓突然造血停滞的现象,又称为再障危象。
本病呈自限性,1个月可自行恢复。

(八)治疗
1、对症治疗:
减轻贫血:输红细胞
控制出血:输血小板,止血剂
防治感染:无菌环境,个人卫生
2、对因治疗:
造血干细胞异常:
促进造血:雄激素 、造血因子
Allo-HSCT (SAA)
免疫异常:免疫抑制剂
CSA
ATG or ALG (SAA)
治疗策略
非重型再障:
促进造血+免疫抑制剂。
重型再障:
免疫抑制剂是主要选择。
尽早考虑干细胞移殖。
(九)小结

四、溶血性贫血
掌握溶贫的定义
熟悉溶贫的分类(病因)
掌握溶贫的诊断(临床表现,实验室检查)
了解溶贫的治疗
自身免疫性溶血(AIHA)
阵发性睡眠性血红蛋白尿(PNH)
(一)定义
溶血:
红细胞非自然衰老而提前遭受破坏的过程。
溶血状态:
骨髓有6-8倍的红系造血代偿能力,如红细胞破坏速率在骨髓代偿范围内,虽有溶血,但不出现贫血,称溶血状态。
溶血性贫血:
指红细胞破坏速率增加,红细胞寿命缩短,超过骨髓造血代偿能力而发生贫血。
正常红细胞寿命约120天,只有在红细胞平均寿命短至15-20天,才会发生贫血。
溶血性黄疸:
溶血伴有黄疸。
髓外造血
生理情况下,出生2月后,肝、脾、淋巴结不再造血,但在病理情况下,如骨髓纤维化,溶血,造血需求增加,骨髓代偿功能不足时,骨髓外的造血组织(肝、脾、淋巴结)重新开始恢复胚胎时期的造血功能。
红细胞形态和膜结构
双凹圆盘状+脂质双层膜→红细胞柔韧性、变形性好,有利于红细胞通过脾窦微血管。
(二)分类

按溶血病程分:
急性溶血:
(多为血管内溶血)输低渗盐水、血型不合输
慢性溶血:
(多为血管外溶血)遗球、地中海贫血
按溶血部位分:
血管内溶血:
阵发性睡眠性血红蛋白尿(PNH)、输低渗盐水、血型不合输血、新生儿溶血
血管外溶血(肝脾内):
AIHA、遗球、地中海贫血
原位溶血(骨髓腔内):
MDS、巨幼贫。本质是血管外溶血。
按病因分:
(一)红细胞内部异常(多为先天性)
1.膜异常:遗传性球形/椭圆形红细胞增多症
2.酶异常:G6PD酶缺乏,丙酮酸激酶缺乏
3.珠蛋白异常:
珠蛋白数量异常:地中海贫血、
珠蛋白结构异常:异常血红蛋白病
4.血红素异常:铅中毒、卟啉病
(二)红细胞外部异常(多为获得性)
1.免疫因素:
AIHA、新生儿溶血症、血型不符的输血
2.血管性:
①微血管病性HA:TTP
②瓣膜病:主动脉狭窄、心脏瓣膜置换术后
③血管壁受反复挤压:行军性血红蛋白尿
3.生物因素:疟疾
4.理化因素:大面积烧伤、亚硝酸盐中毒
(三)病理生理
正常衰老的红细胞破坏的部位


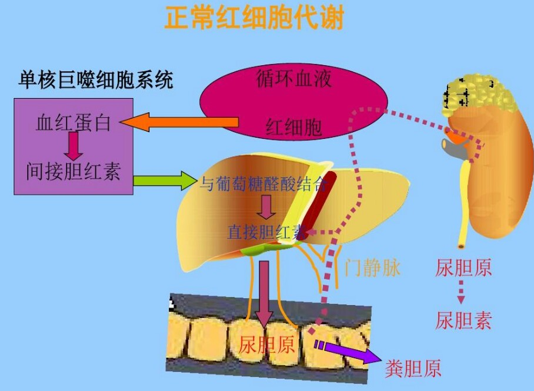
血管外溶血

血管内溶血

尿胆素&尿胆原

(四)临床表现
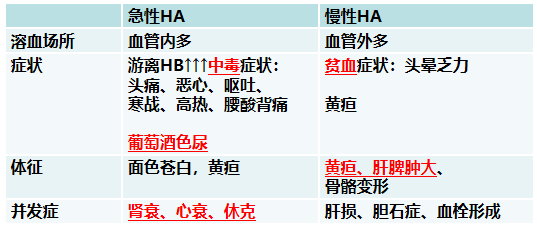
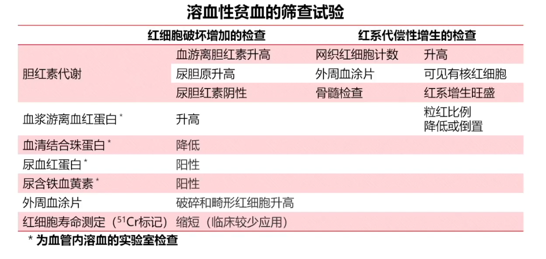
(五)实验室检查
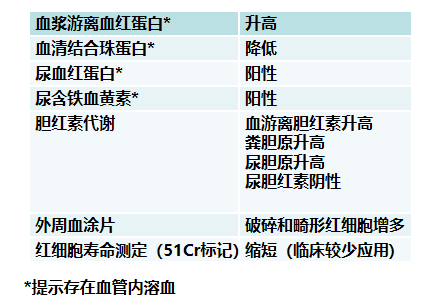
筛查试验:确定溶血及溶血部位
红细胞破坏增加(因)的检查
红系代偿性增生(果)的检查
一、确定溶血及溶血部位
1.红细胞破坏增多的证据
(1)红细胞寿命缩短、破坏增加
①51Cr标记,测红细胞半衰期:最直接的证据,但临床不实用。
正常红细胞T1/2 25-32天,HA 红细胞T1/2 <15天
②红细胞形态改变
球形、椭圆形、盔形、破碎
③LDH↑↑↑:
(2)血浆游离血红蛋白升高(血管内溶血)
①游离HB与HP(结合珠蛋白)结合→结合珠蛋白↓
②游离HB转变为高铁HB,与白蛋白结合→高铁血红素白蛋白
③大部分游离HB经肾代谢→血红蛋白尿→肾小管上皮细胞重吸收
→含铁血黄素→随着肾小管上皮细胞脱落→含铁血黄素尿(尿Rous test +)
(3)胆红素代谢异常
①血清非结合胆红素↑
②粪胆原↑
③尿胆原↑
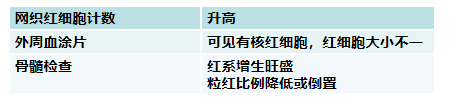
2.红细胞代偿性增生的证据
(1)外周血网织红↑
(2)外周血涂片:
有核红细胞增多
红细胞大小不均匀,嗜多色性,
Howell-Jolly小体,Cabot环
(3)骨髓象:
红系增生明显活跃,粒红比例降低或倒置
HA的筛查实验
二、确定溶贫原因
1红细胞膜缺陷的检查
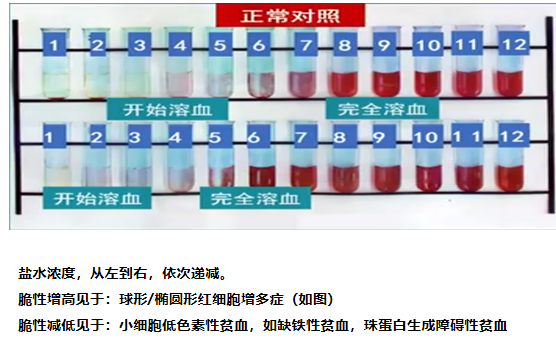
红细胞渗透脆性试验
红细胞特殊形态
血细胞表面CD59、CD55抗原
FLARE检测
酸溶血试验(Ham试验)
2红细胞酶缺陷的检查
G-6-PD酶活性测定
PK酶活性测定
3珠蛋白合成异常的检查
血红蛋白电泳
异丙醇沉淀试验
镰变试验
4免疫性溶血的检查
抗人球蛋白试验(Coombs试验)
继发性AIHA的原发病检查
淋巴细胞增值性疾病:淋巴结超声,CT,PET-CT,病理检查
自身免疫病:抗核抗体系列,类风湿因子等
感染:病毒血清学抗体
实体瘤:肿瘤标记物,影像学检查,病理检查
特殊检查:明确溶血原因
红细胞渗透脆性试验
抗人球蛋白试验(Coombs试验)
酸化血清溶血试验(Ham试验)




(六)溶贫的诊断
病史
1、先天性:自幼发病,类似家族史
2、后天获得性: 成年后起病,无家族史
机械损伤: 人工瓣膜,行军性Hb尿
生物因素: 疟疾 ,严重细菌感染,蛇毒
化学因素: 烧伤,亚硝酸盐中毒,铅中毒
睡眠相关: PNH
药物:
G6PD缺乏症——(氧化剂)抗疟药(奎宁);解热镇痛药(阿司匹林);
AIHA——头孢菌素;嘌呤类似物
食物:蚕豆
气温:寒冷
输血史:
鉴别诊断
其他引起网织红细胞增多的增生性贫血:
失血,缺铁性贫血,巨幼贫
其他引起黄疸的疾病:
梗阻性黄疸、Gilbet综合征
(七)溶贫的治疗
(不是重点,了解即可)
1去除病因
药物诱发的HA,应立即停药并避免再次用药;
冷抗体型自身免疫性HA,应注意防寒保暖;
G6PD酶缺乏患者,应避免使用蚕豆或服用氧化性药物;
怀疑有溶血性输血反应,应立即停止输血,开放补液通路,激素抗过敏,扩容升压。再查明原因;
感染可引起或加重原有的溶血缺陷,应防治感染。
2终止溶血
糖皮质激素:对于温抗体型AIHA具有较好的疗效;对于频发型PNH可减轻溶血发作。(首选)
大剂量丙种球蛋白:起效快,不作用持久
免疫抑制剂:环孢菌素A,他克莫司对某些糖皮质激素治疗无效的温抗体型或冷抗体型AIHA可能有效。
单克隆抗体:抗CD20单克隆抗体可应用与AIHA的二线治疗;抗补体C5单克隆抗体可用于PNH的治疗。
血浆置换:TTP,HUS溶血尿毒综合征,严重顽固的AIHA可考虑血浆置换
右旋糖酐铁:作用弱
3纠正贫血:成分输血
输血可改善贫血症状,减少异常红细胞生成,缓解髓外造血,避免骨骼改变与发育迟缓。
对AIHA输血可能会带来严重反应,如溶血急性发作或加重原有的溶血,有时可引起血栓。输血慎用,指征从严掌握,视为挽救生命的措施,维持HB>6g/dl。
如要输血,一般输洗涤红细胞。
长期输血依赖致血色病。
4切脾
适用于异常红细胞主要在脾破坏者。
遗传性球形细胞增多症是绝对适应症。(6岁以下,不宜切脾)
丙酮酸酶缺乏及地中海贫血,切脾可减轻红细胞破坏,减轻贫血症状。
对需要较大剂量糖皮质激素维持治疗的AIHA。
5补充造血原料
溶血患者骨髓造血代偿性加速,对造血原料的需求增加。
某些慢性HA叶酸消耗增加,应额外补充叶酸;
长期血红蛋白尿患者铁丢失增加,证实缺铁后,应适当补充,但对PNH患者补铁需慎重。
6并发症处理
严重的急性血管内溶血可造成急性肾衰,休克,电解质紊乱等致命并发症,应积极处理。
伴有血栓形成的PNH患者,应给予抗凝治疗。
(八)自身免疫性溶血性贫血(AIHA)
定义
由于免疫功能紊乱,机体产生自身红细胞抗体,红细胞吸附自身抗体和/补体,通过抗原抗体反应,使红细胞破坏加速,引起溶血性贫血。
属于血管外溶血。
最常见的一种后天获得性HA
也是最重要的一种免疫性HA。
病理生理基础
患者体内产生了针对红细胞膜抗原的自身抗体,这种抗体与红细胞膜表面抗原结合使红细胞致敏,致敏红细胞易在单核-巨噬细胞系统内被吞噬破坏,导致血管外溶血的发生;
另外,致敏红细胞还可通过补体激活,引起血管内溶血。
分类:
根据抗体作用与红细胞的最佳温度分为:
温抗体型(warm AIHA,WAIHA)
冷抗体型
混合型AIHA
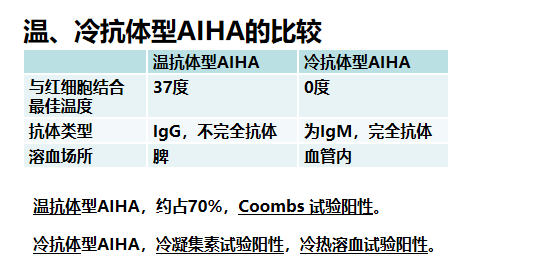
病因

临床表现
血管外溶血:
慢性经过:贫血,黄疸,肝脾肿大(轻中度)
急性发作:溶血危象,再障危象
继发性AIHA可有原发病表现
Evans综合征:
(10-20%)AIHA同时或相继发生免疫性血小板减少症
实验室检查
血常规: HB↓ RET↑
溶血危象时, RET ↑ ↑ ↑ 可达0.5;
急性溶血阶段白细胞可增高
外周血涂片可见球形红细胞、幼红细胞
再障危象时,全血细胞减少
骨髓检查:
红系明显增生,中幼红↑,晚幼红↑
部分红细胞可见Howell-Jolly小体,Cabot环
再障危象时,三系增生减低
Coombs’ test:阳性(确诊试验)
肝功能:非结合胆红素↑
尿常规:尿胆原↑
明确AIHA的原发病:抗核抗体,病毒抗体等
诊断
诱因:近期有输血、特殊药物应用史
HA临床表现
Coombs’ test 阳性
寻找继发性AIHA的病因
治疗
诱因:近期有输血、特殊药物应用史
HA临床表现
Coombs’ test 阳性
寻找继发性AIHA的病因
病因治疗:治疗原发病是根本
一线治疗:肾上腺糖皮质激素:
机理:抑制抗体产生;降低抗原抗体的亲和力;减少巨噬细胞表面IgG、C3受体数量及抑制受体与红细胞结合。
剂量:泼尼松1-1.5mg/(kg.d),急口服性溶血,可用甲强龙。
原则:起始剂量要足,疗程长,贫血纠正后,治疗剂量维持1月,缓慢减量。
副作用:长期激素治疗期间,注意激素副作用。
二线治疗:激素无效,激素禁忌的难治性AIHA
大剂量丙种球蛋白:起效快,不作用持久
其他免疫抑制剂:CSA,FK506
单克隆抗体:抗CD20单抗
切脾:脾脏是产生抗体,破坏致敏红细胞的场所。
血浆置换:迅速降低患者体内的游离抗体,对吸附在红细胞表面的抗体效果不佳
(九)阵发性睡眠性血红蛋白尿(PNH)
定义
是红细胞获得性的膜缺陷克隆性疾病,对补体异常敏感的一种血管内溶血。
临床上表现为:与睡眠有关的间歇发作的血红蛋白尿,可伴有全血细胞减少和/或反复血栓形成。
发病机制
1.PNH造血干细胞内的PIG-A基因发生突变(克隆性疾病)。
2.GPI锚连膜蛋白丢失, 其中最要的是CD55,CD59→导致细胞膜的缺陷,细胞膜稳定性↓。
3.红细胞对补体致敏性增加→ 血管内溶血。
4.异常免疫损伤正常造血干细胞 →导致造血功能衰竭(PNH-AA综合征)

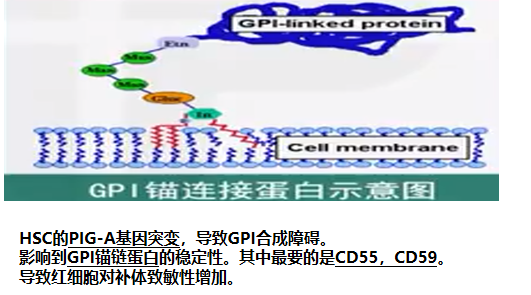
分型
CD59:
反应性溶血膜抑制复合物,阻止膜攻击复合物的组装。
CD55:
衰变加速因子,抑制C3转化酶的形成及稳定。
以流式细胞术检测CD59-红细胞,根据缺失CD59的程度区分对补体敏感程度不同的红细胞群:
PNH I型,正常;
PNH II型,部分缺失;
PNH III型,完全缺失。
临床表现

实验室检查


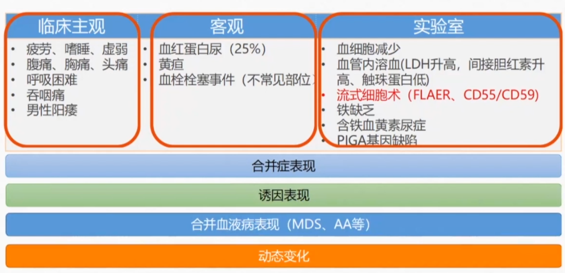
诊断

分类

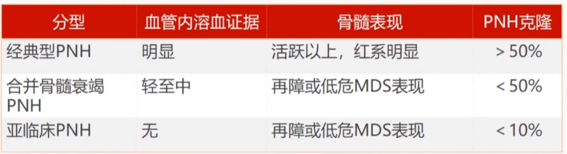
治疗
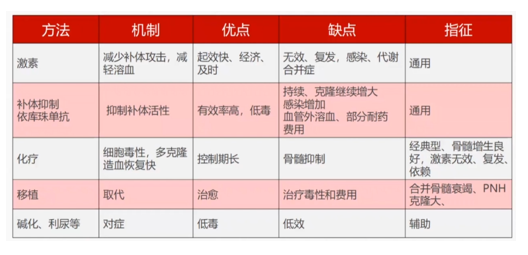
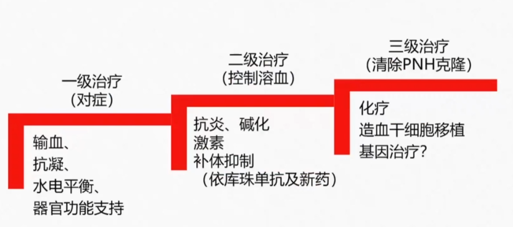
避免诱因:感染,某些药物。
控制溶血:糖皮质激素,抗补体单克隆抗体Eculizumab
并发症治疗:碳酸氢钠碱化,低分子肝素,阿司匹林
异基因造血干细胞移植:
其他:输血,雄激素,铁剂
预后
血栓,出血,感染是主要的死亡原因。
少数转变为急性白血病、MDS。
小结

思考题
溶血性贫血的病因?
溶血性贫血的临床表现?
溶血性贫血的实验室检查?